今年3月,來自恒瑞源正的研發團隊在Nature Communications雜志(影響影子16.6)上發表題為HLA-class II restricted TCR targeting human papillomavirus type 18 E7 induces solid tumor remission in mice的研究論文。詳細介紹了公司首個進入臨床階段的TCR-T產品(HRYZ-T101)的研發過程、作用機制和臨床前藥效毒理等研究結果。HRYZ-T101為全球首創新藥(First in class),屬于國內外均未上市的新靶點,新結構,新機制創新藥。

研究發表于Nature Communications雜志
01 研究背景
宮頸癌(Cervical Cancer)是婦科常見的惡性腫瘤之一,發病率在女性惡性腫瘤中居第四位,目前國內外對于二線化療失敗的轉移或復發性宮頸癌患者尚無可推薦的治療方案。研究證實,95%以上的宮頸癌均與HPV(人乳頭瘤病毒)相關,其中以16型和18型最為常見。此外,HPV感染還會導致多種頭頸癌和肛門生殖器腫瘤。HPV感染后癌變的腫瘤細胞中會持續性高表達E7病毒蛋白,此蛋白在正常組織中不表達,是TCR-T等靶向治療的優良靶點。
02 研究結果
本研究中,科研團隊基于TCR逆向基因工程(Reverse Genetic Engineering of TCR,ReGET)平臺技術,成功地從一位早期多抗原自體免疫細胞治療(MASCT)獲益患者體內克隆到靶向HPV18 E7腫瘤抗原的TCR分子(10F04 TCR)。該患者在2011年被診斷為HPV陽性晚期轉移性宮頸鱗狀細胞癌,經手術、化療、放療等常規治療后復發。患者于2014年起,經過多療程MASCT治療后腫瘤逐漸消退并獲得長期緩解,截至目前已無瘤生存超過九年。該患者體內針對HPV18 E7等多種腫瘤抗原特異性T細胞的長期存在是該患者臨床獲益的可能原因。
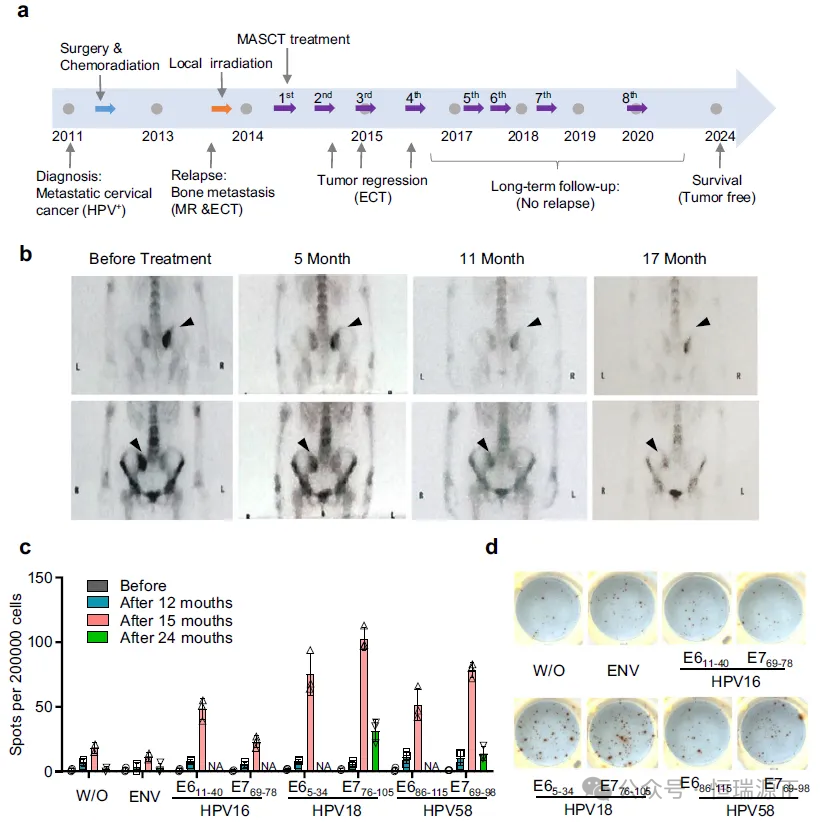
MASCT免疫獲益患者治療概況及免疫相應
研究結果證實,10F04 TCR特異性識別中國人群高頻的HLA-II分子HLA-DRB1*09:01遞逞的HPV18 E7抗原肽,在體外和小鼠模型中均展現了強大的抗腫瘤活性。結果顯示,10F04 TCR可同時介導CD4 和CD8 T細胞中實現對抗原陽性腫瘤細胞的識別和直接殺傷,并釋放IFNγ, TNFα, IL2, Granzyme B等抗腫瘤細胞因子,進一步誘導腫瘤細胞凋亡并促進TCR-T細胞的擴增。同時,激活的TCR-T細胞分泌的IFNγ細胞因子也能誘導腫瘤表面HLA分子的表達上調,使其對TCR-T的識別更加敏感。近年來,越來越多的臨床研究結果表明,CD4 腫瘤識別T細胞在腫瘤治療中起到關鍵性的作用,通過直接殺傷,輔助CD8 T細胞的殺傷和長期存續,以及分泌細胞因子等途徑調動DC,巨噬細胞等固有免疫系統實現針對腫瘤的抗腫瘤作用。本研究報道的10F04 TCR分子可實現CD4 和CD8 T細胞的同時激活并能分泌多種細胞因子;同時,本研究也對人類蛋白質組和主要HLA分子進行了交叉識別驗證,未發現10F04TCR任何脫靶風險。
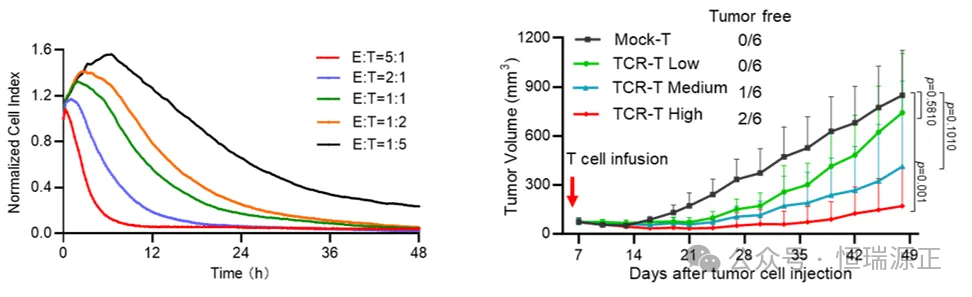
10F04 TCR-T細胞臨床前藥效
03 后續進展
目前,HRYZ-T101產品已獲得CDE批準用于HPV18陽性實體瘤的治療,I期注冊臨床試驗已完成首例患者回輸。I期注冊臨床試驗中心在復旦大學附屬腫瘤醫院、華中科技大學同濟醫學院附屬協和醫院、鄭州大學第一附屬醫院,正在招募中。



參考文獻:
[1] Long, J. et al. HLA-class II restricted TCR targeting human papillomavirus type 18 E7 induces solid tumor remission in mice. Nature Communications 15, 2271 (2024).
